
Seit dem Inkrafttreten der MDR (Medizinprodukteverordnung 2017/745) und der IVDR (Verordnung für In-vitro-Diagnostika 2017/746) im Mai 2021 müssen sich sowohl Hersteller und Bevollmächtigte als auch Importeure in EUDAMED registrieren, der neuen europäischen Datenbank für Medizinprodukte (European Database on Medical Devices).
Die Datenbank soll unter anderem als Registrierungs-, als Melde- und als Verbreitungssystem (in Teilen öffentlich zugänglich) fungieren. Dadurch soll der europäische Markt für Medizinprodukte transparenter, die Qualität der Produkte erhöht und die Koordination von Informationen zu Medizinprodukten vereinfacht werden. Die Datenbank wird aus sechs miteinander verbundenen Modulen bestehen.
Durch die Registrierung in EUDAMED erhalten Wirtschaftsakteure eine SRN, eine sogenannte Single Registration Number, die in Artikel 31 Absatz 2 der MDR vorgeschrieben ist.
Sie benötigen für die Registrierung ein Bestätigungsdokument der unternehmerischen Tätigkeit. Bei diesem Bestätigungsdokument kann es sich zum Beispiel um einen Handelsregisterauszug oder auch eine Gewerbeanmeldung handeln.
Was ist ein Wirtschaftsakteur?
Wirtschaftsakteure sind natürliche oder juristische Personen, die durch Handlungen einen Einfluss auf den Verlauf der wirtschaftlichen Entwicklung nehmen. Für EUDAMED werden diese Rollen unterschieden:
- Hersteller (MF – Manufacturer)
- Autorisierter Vertreter bzw. Bevollmächtigter (AR – Authorised Representative)
- Hersteller von System- und Behandlungseinheiten (PR – System & Procedure Pack Producer)
- Importeur (IM – Importer)
Sollte ein Wirtschaftsakteur mehrere Rollen zeitgleich einnehmen, erfolgt eine Registrierung für jede dieser Rollen.
- Beispiel 1: Die Organisation A befindet sich in Österreich und ist Hersteller eines Medizinprodukts. Dementsprechend wird diese Rolle in EUDAMED registriert und die SRN könnte so aussehen: AT-MF-000000001
- Beispiel 2: Die Organisation B befindet sich in Deutschland, stellt ein Medizinprodukt her und importiert weitere Medizinprodukte. Dementsprechend wird jede Rolle einzeln in EUDAMED registriert und die Organisation B könnte diese SRN erhalten: DE-MF-000000002 und DE-IM-000000003
Was ist eine Single Registration Number?
Durch die Registrierung eines Wirtschaftsakteurs in EUDAMED erhält dieser eine Single Registration Number (SRN). Die SRN dient dazu, Wirtschaftsakteure eindeutig zu identifizieren und wird nach erfolgreich abgeschlossener Registrierung vergeben.
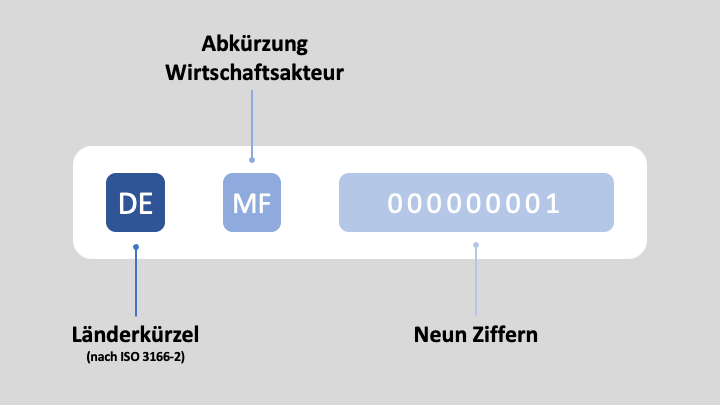
Die SRN besteht aus drei Teilen: dem Länderkürzel nach ISO 3166-2, der Abkürzung der Art des Wirtschaftsakteurs und neun Ziffern.
Welche Module gibt es und wie ist der Stand der Dinge?
Das erste Modul, zur Registrierung von Wirtschaftsakteuren, wurde bereits im Dezember 2020 freigeschaltet. Die nächsten Module, zur Registrierung der UDI bzw. von Medizinprodukten sowie das Modul „Benannte Stellen und Zertifikate“, sollen ab dem September 2021 zur Verfügung stehen. Weitere Module sollen schrittweise implementiert werden. Die sechs Module in der Übersicht:
- Registrierung von Wirtschaftsakteuren
- UDI-Datenbank / Registrierung von Produkten
- Benannte Stellen und Bescheinigungen
- Klinische Prüfungen und Leistungsstudien
- Vigilanz und Überwachung nach dem Inverkehrbringen
- Marktüberwachung
Sie haben Fragen zur Registrierung in EUDAMED? Kontaktieren Sie uns für eine kostenfreie Erstberatung, für Unterstützung bei der Registrierung in EUDAMED bzw. auftretenden Fragen rund um die Zulassung Ihrer Medizinprodukte
